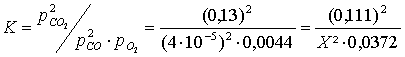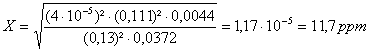Brennstoffverbrennung
Typologisierung der Verbrennungen
Verbrennungsreaktionen
Globalreaktionen
Elementarschritte
Reaktion und Dissoziation, Reaktionsrichtung
Einführung in die Brennerkonstruktion
Flammentemperatur, Verbrennungstemperatur
Zündtemperatur und Flammenstabilität
Schadstoffarme Gasbrennerkonstruktionen
Schadstoffarme Ölbrennerkonstruktionen
Lösung der Aufgaben
Lösung der Aufgaben
Aufgabe 1: Ermitteln Sie den Abgastaupunkt der Verbrennungsprodukte der Reaktionen nach Gln (10) und (11) mit Hilfe von Tabelle 1 oder Abbildung 2!
Abgas der Verbrennung nach Gl (10): 66.67% N2 + 33.33 % H2O
Abgas der Verbrennung nach Gl (11): 9,1 % CO2 + 18,2 % H2O + 72,7% N2
|
Sättigungstemperatur °C |
Sättigungsdruck Pa |
Sättigungskonzentration % H2O |
|
50 |
12334 |
12,3 |
|
60 – 0,612 = 59,388 |
|
18,2 Gl. (10) |
|
60 |
19919 |
19,1 |
|
70 |
31161 |
31,2 |
|
70 + 1,3 = 71,3 |
|
33,33 Gl. (11) |
|
80 |
47359 |
47,4 |
18,2 = 19,1 – 0,9 19,1 - 6,8 = 12,3
60°C 50°C
10 ,0K 6,8
0,9 K X X = ( 0,9 * 6,8 ) / 10,0 = 0,612 K
2,13 16,4
X 10 X = 21,3 / 16,4 = 1,3
Aufgabe 2: Ermitteln Sie die Zusammensetzung der „trockenen“ Abgase der Reaktionen nach Gln (10) und (11)!
Abgas der Verbrennung nach Gl (10): 66.67% N2 + 33.33 % H2O
Abgas der Verbrennung nach Gl (10): 9,1 % CO2 + 18,2 % H2O + 72,7% N2
Gl. (10) Trocken: 100 % N2
Gl. (11) Trocken: 9,1 CO2 + 72,7 N2 = 81,8
9,1 / 81,8 72,7 / 81,8
11,1 % CO2 + 88,9 % N2 = 100 %
Aufgabe 3: Ermitteln Sie die Zusammensetzung der trockenen Abgase nach Tabelle 3!
|
Luftzahl |
Abgas |
CO2 |
H2O |
N2 |
O2 |
S |
Taupunkt |
|
l=1,0 |
Volumenanteil (feucht) |
0,95 |
1,9 |
7,65 |
58 [°C] |
||
|
[%] (feucht) |
9,05 |
18,1 |
72,86 |
||||
|
l=1,1 |
Volumenanteil (feucht) |
0,95 |
1,9 |
8,41 |
55 [°C] |
||
|
[%] (feucht) |
8,3 |
16,52 |
73,13 |
||||
|
l=1,3 |
Volumenanteil (feucht) |
0,95 |
1,9 |
9,93 |
52 [°C] |
||
|
[%] (feucht) |
7,11 |
14,23 |
74,38 |
||||
|
l=1,5 |
Volumenanteil (feucht) |
0,95 |
1,9 |
11,45 |
49 [°C] |
||
|
[%] (feucht) |
6,23 |
12,46 |
75,08 |
Tabelle 3: Berechnung der Abgastaupunkt nach Beispiel Nr. 1
|
Luftzahl |
Abgas |
CO2 |
N2 |
O2 |
S |
|
l=1,0 |
Volumen (trocken) |
0,95 |
7,65 |
||
|
[%] (trocken) |
11,05 |
88,95 |
|||
|
l=1,1 |
Volumen (trocken) |
0,95 |
8,41 |
||
|
[%] (trocken) |
9,95 |
88,06 |
|||
|
l=1,3 |
Volumen (trocken) |
0,95 |
9,93 |
||
|
[%] (trocken) |
8,3 |
86,72 |
|||
|
l=1,5 |
Volumen (trocken) |
0,95 |
11,45 |
||
|
[%] (trocken) |
7,17 |
86,42 |
Aufgabe 4: Berechnen Sie die fehlenden Werte in Tabelle 5 unter Zugrundelegung der Tabellen 1, 2 und 4 und der Abbildung 2!
|
Zusammensetzung |
Heizöl |
Erdgas L |
Erdgas H |
|
Gew.-% |
Vol.-% |
Vol.-% |
|
|
Kohlenstoff (C) |
86 |
|
|
|
Wasserstoff (H) |
13 |
|
|
|
Stickstoff (N) |
0,5 |
14 |
1 |
|
Schwefel (S) |
0,3 |
|
|
|
Methan (CH4) |
|
82 |
93 |
|
Kohlenwasserstoffe (C2H6) |
|
3 |
5 |
|
ABGASWERTE |
|||
|
CO2, max. % |
15,5 |
10,3 |
|
|
Lmin. m³/kg |
11,1 |
8,37 |
|
|
Vmin. trocken m³/kg |
10,4 |
7,64 |
|
|
Vmin. feucht m³/kg |
11,8 |
9,37 |
|
|
Abgastaupunkt λ = 1,05 °C |
48,6 |
57,8 |
|
|
Abgastaupunkt λ = 1,1 °C |
47,8 |
56,9 |
|
|
Abgastaupunkt λ = 1,2 °C |
46 |
54,9 |
|
|
Abgastaupunkt λ = 1,4 °C |
43 |
51,9 |
|
Tabelle 5 Feuerungstechnische Kennzahlen von Erdöl und Erdgas
Heizöl:
|
Brennstoff-Komponente |
Anteil |
Luftbedarf m³ / kg |
Abgas m³ / kg |
|
|
C |
0,86 |
7,65 |
1,61 CO2 |
|
|
H |
0,13 |
3,44 |
1,44 H2O |
|
|
S |
0,005 |
0,01 |
0,002 SO2 |
|
|
N |
0,005 |
0 |
0,004 N2 |
|
|
Lmin. |
|
11,1 |
11,1*0,79 N2 |
|
|
Vmin. feucht |
|
|
11,8 |
|
|
Vmin. trocken |
|
|
10,4 |
|
|
CO2, max,trocken |
|
|
15,5 |
|
|
V λ. feucht λ = 1,05; 1,1; 1,2; 1,4 |
12,4 |
12,9 |
14 |
16,2 |
´
|
H2O % λ = 1,05; 1,1; 1,2; 1,4 |
11,6% |
11,2% |
10,3% |
8,89% |
|
Taupunkt λ = 1,05; 1,1; 1,2; 1,4 |
48,6°C |
47,8°C |
46°C |
43°C |
Heizöl-Taupunkt, lineare Interpolation
|
Taupunkt |
50 °C |
40 °C |
48,57 |
47,76 |
45,92 |
43,04 |
|
Sättigung |
12,3% |
7,4 % |
11,6 |
11,2 |
10,3 |
8,89 |
|
∆Sättigung |
12,3 – 7,4 = 4,9 % |
11,6-7,4= 4,2 |
3,8 |
2,9 |
1,49 |
|
|
∆Taupunkt |
50 – 40 = 10 °C |
4,2*10/4,9=8,57 |
7,76 |
5,92 |
3,04 |
|
Erdgas H: 82 % CH4; 3 % C2H6; 14% N2 Luft: 21 % O2% , 79 % N2
CH4 + 2 O2 + 2(79/21) N2 ® CO2 + 2 H2O + 2(79/21) N2
CH4 + 2 O2 + 7,59 N2 ® CO2 + 2 H2O + 7,59 N2
C2H6 + 3,5O2 + 3,5(79/21) N2 ® 2 CO2 + 3 H2O + 3,5(79/21) N2 C2H6 + 3,5O2 + 13,2 N2 ® 2 CO2 + 3 H2O + 13,2 N2
|
Stöchiometrische Methan- und Ethanverbrennung |
|||||||||||||||
|
1 |
CH4 |
+ |
2 O2 |
+ |
7,59 N2 |
|
|
Þ |
CO2 |
+ |
2 H2O |
+ |
7,59 N2 |
|
|
|
2 |
C2H6 |
+ |
3,5 O2 |
+ |
13,2 N2 |
|
|
Þ |
2CO2 |
+ |
3 H2O |
+ |
13,2 N2 |
|
|
|
Stöchiometrische Erdgasverbrennung |
|||||||||||||||
|
3 |
0,82× CH4 0,03 C2H6 |
+ |
0,82×2 0,03×3,5 =1,75 O2 |
+ |
0,82×7,59 0,03×13,2 = 6,62 N2 |
+ |
0.14 N2 |
Þ |
0,82 0,03× 2 = 0,88 CO2 |
+ |
0,82×2 0,03×3 = 1,73 H2O |
+ |
= 6,62 N2 |
+ |
0.14 N2
|
|
4 |
1 m³ Erdgas |
+ |
8,37 m³ Luft |
Þ |
9,37 m³ Abgas ( mit 0,88 m³ CO2 und 1,73 m³ H2O) H2O =18,5 % |
||||||||||
|
5 % Luftüberschuss |
|||||||||||||||
|
5 |
1 m³ Erdgas |
+ |
8,79 m³ Luft |
Þ |
9,79 m³ Abgas ( mit 0,88 m³ CO2 und 1,73 m³ H2O ) H2O =17,7 % |
||||||||||
|
10 % Luftüberschuss |
|||||||||||||||
|
6 |
1 m³ Erdgas |
+ |
9,21 m³ Luft |
Þ |
10,2 m³ Abgas ( mit 0,88 m³ CO2 und 1,73 m³ H2O ) H2O =17 % |
||||||||||
|
20 % Luftüberschuss |
|||||||||||||||
|
6 |
1 m³ Erdgas |
+ |
10 m³ Luft |
Þ |
11 m³ Abgas ( mit 0,88 m³ CO2 und 1,73 m³ H2O ) H2O = 15,7 % |
||||||||||
|
40 % Luftüberschuss |
|||||||||||||||
|
6 |
1 m³ Erdgas |
+ |
11,7 m³ Luft |
Þ |
12,7 m³ Abgas ( mit 0,88 m³ CO2 und 1,73 m³ H2O ) H2O = 13,6 % |
||||||||||
Erdgas L -Taupunkt, lineare Interpolation
|
Taupunkt |
50 °C |
60 °C |
51,88 |
54,93 |
56,81 |
57,83 |
|
Sättigung |
12,3% |
19,1 % |
13,6 |
15,7 |
17 |
17,7 |
|
∆Sättigung |
6,9 % |
1,3 |
3,4 |
4,7 |
5,4 |
|
|
∆Taupunkt |
10 °C |
1,88 |
4,93 |
6,81 |
7,83 |
|
 |
Aufgabe 6: Bei einer Verbrennung befindet sich die Flamme im Dissoziationsgleichgewicht. Die Zusammensetzung des Abgases ist:
Aufgabe 7: Welcher Anteil des Brennstoffschwefels ist als Schwefeldioxid und als Schwefeltrioxid bei der Verbrennung mit 2 % und mit 20 % Luftüberschuss vorhanden, wenn sich die Schwefeloxide im Dissoziationsgleichgewicht befinden?
K 1000 °C = SO32/( SO22×O2)= 0,0277
λ = 1,02
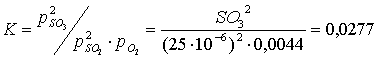
![]()
SOx = SO2+ SO3
SO2= 25 ppm, SO3= 55,2 ppm, SOx = SO2 +SO3= 80,2 ppm
SO2=25/80,2 = 31,2 %
λ = 1,2
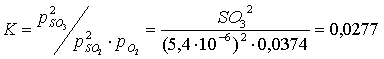
![]()
SOx = SO2+ SO3
SO2= 5,4 ppm, SO3= 74,6 ppm, SOx = SO2 +SO3= 80,0 ppm
SO2=5,4/74,6 = 7,2 %
Aufgabe 8: Warum steigt die NO-Bildung, und warum sinkt die CO2–, SO3– und H2O–Bildung mit zunehmender Verbrennungstemperatur?
Antwort: Die NO-Bildung ist endotherm, die CO2–, SO3– und H2O–Bildungsreaktionen sind exotherm. Die Regel nach le Chatelier besagt, dass die Reaktionsrichtung immer diejenige ist, welche die Extremwerte mindert. Ist die Flammentemperatur zu hoch, so werden die Reaktionsrichtungen gefördert, die einen weiteren Anstieg der Flammentemperatur verhindern.
Aufgabe 9: In welche Richtung verschiebt sich die Dissoziationslinie der Schwefelverbrennung bzw. Schwefeloxiddissoziation bei einer starken Zunahme des Feuerraumdruckes?
Antwort: . Die Regel nach le Chatelier besagt, dass die Reaktionsrichtung immer diejenige ist, welche die Extremwerte mindert. Die Globalreaktion der Schwefelverbrennung bzw. Schwefeloxiddissoziation lautet:
![]()
Bei der Verbrennung entstehen aus 3 Molekülen (2 SO2 und 1 O2 ) 2 Moleküle (2 SO3).
Die Reaktion führt also bei konstantem Feuerraumdruck zu einer Druckminderung. Einer Erhöhung des Feuerraumdruckes wirkt die Druckminderung entgegen: Also wird die Reaktion der SO3–Bildung begünstigt; Die Reaktionsrichtung verschiebt sich rechts in Gleichung (20), die Dissoziationslinie verschiebt sich rechts in Abbildung (5).
Aufgabe 10: Interpretation der Tabellen 5a, 5b und 5c.
a) Wie hoch ist die CO-Konzentration bei 10 % Luftüberschuss bei homogener Brennstoff-Luft-Mischung im Abgas eines Heizkessels mit einer Feuerraum-Endtemperatur von 1500 K?
b) Wie hoch ist die CO-Konzentration bei 10 % Luftüberschuss bei homogener Brennstoff-Luft-Mischung im Abgas eines Heizkessels mit einer Feuerraum-Endtemperatur von 1700 K?
c) Wie hoch ist die CO-Konzentration bei 20 % Luftüberschuss bei inhomogener Brennstoff-Luft-Mischung im Abgas eines Heizkessels mit einer Feuerraum-Endtemperatur von 1700 K, wenn in der einen Feuerraumhälfte 10% Luftmangel und in der anderen Feuerraumhälfte 50% Luftüberschuss herrschen?
a) Tabelle 5a, λ=1,1 1500 K CO = 5 ppm
b) Tabelle 5a, λ=1,1 1700 K CO = 60 ppm
c) Tabelle 5c, λ=0,9 1700 K 31840 ppm
Tabelle 5c, λ=1,5 1700 K 20 ppm
(31840 + 20) / 2 = 15920 ppm
Aufgabe 11: Bei einer Verkleinerung der Brennerleistung wird der Luftzahlbereich, in dem eine zufrieden stellende Verbrennung möglich ist, bei Heizölfeuerung insbesondere bei der Leistung unterhalb ca. 15 kW immer kleiner, siehe Abbildung 7.
Wie erklären Sie es?
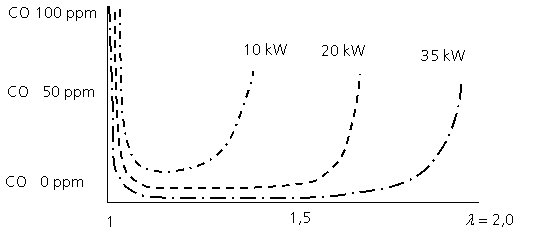 |
Abbildung 7: Einfluss der Luftzahl auf die Kohlenmonoxid-Konzentration im Abgas bei der Verbrennung von Heizöl EL für verschiedene Brennerleistungen
Lösung:
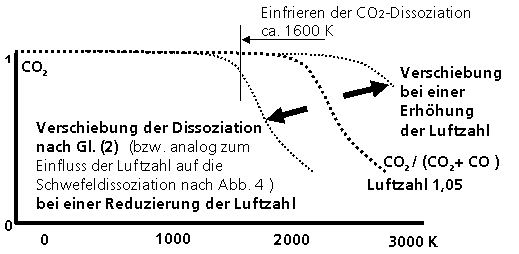 |
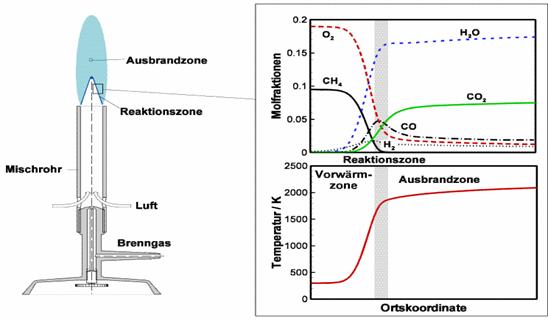
Einfluss der Änderung der Luftzahl auf die Dissoziation von CO2 in Analogie zu Abbildung 4
Bei einer Reduzierung der Luftzahl erhöht sich die CO-Konzentration nach den Dissoziationsgleichungen (12) und (13). Die Erhöhung der CO-Konzentration ist unabhängig von der Brennerleistung. Die Luftzahl, bei der die CO-Konzentration ca. 40 ppm überschreitet, ist im Diagramm der Aufgabenstellung bei allen drei Brennerleistungen ca. 1, 05.
zu wenig Luft Þ unvollständige Verbrennung Þ viel CO
Bei einer Erhöhung der Luftzahl sinkt die Verbrennungstemperatur. Insbesondere bei kleinen Brennerleistungen wird der Luftzahlbereich immer kleiner, in dem die Verbrennungstemperatur ca. 1600 K übersteigt. Dies ist die Temperatur, bei der die CO-Dissoziation einfriert, und zugleich die Mindesttemperatur für eine vollständige CO-Verbrennung bei Hausheizungen.
Die Luftzahl, bei der 1600 K Verbrennungstemperatur unterschritten wird, beträgt in Abbildung 4 ca. 1,3, 1,6 und 1,8 für die Brennerleistungen 10, 20 und 35 kW. Die Luftzahl, bei der die CO-Konzentration ca. 40 ppm überschreitet, beträgt nach Abbildung 6 bei den drei Brennerleistungen ebenfalls ca. 1,3, 1,6 und 1,8.
zu viel Luft Þ zu niedrige Verbrennungstemperatur Þ unvollständige
Verbrennung Þ viel CO, insbesondere bei kleiner Brennerleistung
Aufgabe 12: Warum ist das Starten eines Verbrennungsmotors schwieriger im Winter als im Sommer?
Im Winter ist der ausgekühlte Motor kälter als im Sommer. Dadurch ist der Löschabstand größer. Dies erschwert den Start des Motors.
Aufgabe 13: Wie gehen Sie vor, wenn bei der Inbetriebnahme einer Heizungsanlage der Brenner nicht zündet?
Bei der Inbetriebnahme sind die Temperaturen der Feuerraumwand und der Brennerbauteile kälter als im ausgestalteten Zustand beim Taktbetrieb. Dies führt zu einer Verminderung der Flammentemperatur und zu einer Vergrößerung des Löschabstandes. Mit einer Verminderung der Luftzahl kann man den Kaltstart verbessern. Gegebenfalls muss zum Kaltstart die Luftzahl so weit reduziert we