TTZ Lampoldshausen
Seminar
24. Mai 2012
74329 Hardthausen-Lampoldshausen
Zoltán Faragó
Verbrennungsvorgänge in Kaminöfen
Wirtschaftsförderung Raum Heilbronn GmbH,
Technologie-Transfer-Zentrum Lampoldshausen,
Deutsches Zentrum für Luft- und Raumfahrt e.V.

Gliederung:
Grundlagen
Chemie der Holzverbrennung
Flammenleuchten – Rußbildung
Lesen aus der Flamme
Formel und Kennzahlen
Optimales Feuern
Warum leuchtet die Flamme?
Das Leuchten der
Flamme hat zwei Ursachen:
1) Wärmestrahlung
heißer Feststoffpartikel (Ruß, Feinstaub, Flugasche)
2) Lichtstrahlung
angeregter Radikale, Ionen und Atome (Chemolumineszenz)
Wärmestrahlung
/ Schwarzkörperstrahlung
Stefan-Boltzmann-Gesetz
![]() (9)
(9)
Plancksches
Strahlungsgesetz

(10)

Bild 14: Spektrale Intensitätsverteilung bei verschiedenen Temperaturen (Quelle: Ronny Puchner, Fotoschule, www.puchner.org)
Die Intensität
und Wellenlänge der Wärmestrahlung ist eine Funktion der Temperatur des
strahlenden Körpers. Die Farbe des glühenden Körpers verrät dessen Temperatur:
800-900°C dunkelrot, 1000°C hellrot, 1100°C Übergang von rot zu orange, 1200°C
orange, 1300-1400°C Übergang orange zu gelb, usw. Die „Farbtemperatur“ ist die
Temperatur des glühenden schwarzen Körpers („Schwarzkörperstrahlung“, Bild 15)

Bild 15: Schwarzkörperstrahlung und Farbtemperatur (K)
Einige typische Werte für die Farbtemperatur: Kerzenlicht 1400 bis 1800 K, Glühbirne 40W 2700 K, 200 W 3000 K,
Sonnenaufgang/Sonnenuntergang 3200K, Halogenlampe 3400 K, Tageslicht 5500 K.
Das menschliche Auge ist in der Lage, die für die Flamme typischen Temperaturen (1000 - 2000 °C) genau zu erkennen. Bereits vor mehreren tausend Jahren konnten Töpfer, Schmiede, Metall- und Glashersteller die Brenntemperatur durch Beobachtung der Flamme auf ± 5°C genau einstellen. In


Bild 16: Links: Spektralanalyse des Tageslichtes an einem trüben Tag; Wellentäler (655, 687, 724, 760 nm u.a.) als Absorptionsspektren von O2 und H2O;
Rechts: Spektralanalyse der Butan-Diffusionsflamme
Lichtstrahlung angeregter Radikale
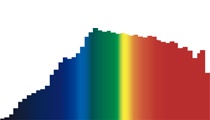
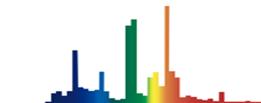
Bild 17: Spektrum des Tageslichtes (links) und der Leuchtstofflampe (rechts)
Die Intensitätsverteilung des „Regenbogens“ verrät die Temperatur des strahlenden Körpers (siehe Bild 17 links). In der Flamme sind die Rußpartikel die strahlenden Körper. Bei einer rußfreien Flamme fehlen die strahlenden Körper, die „Originalfarbe“ der Flamme kommt zur Geltung. Die Spektrallinien der Leuchtstofflampe (Bild 17 rechts) verraten die Zusammensetzung des leuchtenden Gases.


Bild 18: Zerlegung des weißen Lichtes mittels einer Spektralfolie; rechts Spektralbrille

Bild 19: Emission von Butan-Vormischflamme, wie gezeigt in Bild 8, zweites Foto von links
(Quelle: http://www.worldofmolecules.com/fuels/butane.htm)
Die Spektrallinien in der blauen Flamme verraten die chemischen Reaktionen (Elementarschritte der Verbrennung, siehe Bild 4). Erste Spektralbilder einer blaubrennenden Kohlenwasserstoffflamme beobachtete der schottische Physiker William Swan 1857 “On the prismatic spectra of the flames of compounds of carbon and hydrogen”). Es war ebenfalls W. Swan, der als erster die gelbe Spektrallinie des Natriums in der Flamme beobachtete. Eine durch Natrium (Kochsalz) gefärbte gelbe Flamme ist in Bild 20 zu sehen.


Bild 20 Methanol-Diffusionsflamme bei Flammenfärbung durch Natrium; links Flammenbild im verdunkelten Raum, rechts Flammenbild durch die Spektralbrille


Bild 21: Butan-Diffusionsflamme im verdunkelten Raum; links ohne, rechts mit Spektralbrille
![]()
![]()



Bild 22: Butan-Diffusionsflamme bei Tageslicht
Bei der Zündung der Kohlenwasserstoff-Flamme bilden sich zunächst CH-Radikale (siehe Gl. (4) und Bild 4). Bild 19 zeigt bei der Wellenlänge ≈430 nm einen deutlichen CH-Peak, welcher für die blaue Farbe der rußfreien Flamme sorgt.
Die Elementarreaktionen der Kohlenwasserstoffverbrennung sind in den Bildern 4 und 5 dargestellt. Die C2H2-Radikale (Ethylenradikale) sind mit roten Pfeilen hervorgehoben. C2H2-Rakikale sind Rußbausteine, Ruß entsteht durch Polymerisation der Ethylenradikale. Nach einer sehr vereinfachten Darstellung in Gleichung (11) verläuft die Rußbildung nach dem Muster:
n⋅C2H2 → C2nHn + 0,5⋅n⋅H2 und (11a)
m⋅ C2nHn → C 2⋅m⋅n + 0,5⋅m⋅n⋅H2 (11b)
Nach dem Reaktionsmuster Gl. (11a) und (11b) wird für die Rußbildung Ethylen (C2H2) benötigt. Ethylen bildet sich in der Flamme während der Verbrennung. Am Anfang der Verbrennung, etwa in der ersten Millisekunde, ist in der Flamme noch kein Ethylen vorhanden (es sei denn, der Brennsoff selbst ist Ethylen), und die Flamme ist blau! Dies ist auch bei rußenden Diffusionsflammen der Fall, wie es beispielsweise in Bild 22 zu beobachten ist: Ein Ein-Millimeter-Spalt über dem Brenner ist eine schwache blaue Flamme zu sehen, erst dann bildet sich Ruß, und die Flamme wird gelb. Ein ähnlicher Effekt ist in den Bildern 21, 8 und 6 zu beobachten.
Bei rußender Flamme verrät die Flammenfarbe die Flammentemperatur. Auch eine nichtrußende Flamme weist eine Flammenfarbe aus, die, je nach Ursache der Flammenfärbung, die gleiche sein kann wie die der rußenden Flamme. In Bild 20 ist die gelbe Farbe durch Flammenfärbung des Natriums verursacht. Würde die gleiche Farbe von Ruß verursacht, würde die Farbe auf eine Flammentemperatur von ca. 1250 °C hinweisen. Dann allerdings würde die Flamme bei Betrachtung durch die Spektralbrille ein Muster in Regenbogenfarben zeigen (Bild 16). Bei Betrachtung der gelbgefärbten Methanolflamme durch die Spektralbrille (Bild 20 rechts) zeigen sich die Flammenbilder der Brechung 1. Ordnung und Brechung 2. Ordnung in gleicher gelben Farbe.



Bild 23: links – Methanolflamme, Flammenfärbung durch Strontium
Mitte – Methanolflamme durch Spektralbrille, Flammenfärbung durch Strontium
rechts – Ethanolflamme durch Spektralbrille, Flammenfärbung durch Ruß
Bild 23 zeigt Flammenbilder im verdunkelten Raum. Beim linken Bild betrüge die Flammentemperatur, wenn die Farbe durch Glühen der Rußpartikel verursacht wäre, ca. 1000 °C. Die Methanolflamme ist aber nicht rußend – sie wird durch Strontium rot gefärbt. Das mittlere Bild zeigt bei jeder Brechung die gleichen Farben, also die Farben entsprechen den Spektrallinien des Strontiums. Das rechte Bild zeigt eine schwach rußende Ethanolflamme, bei der die Spektralbilder die Regenbogenfarben beinhalten. In diesem Fall zeigt die Flammenfarbe die Flammentemperatur (ca. 1100 °C).





Bild 24: Oben, von links nach rechts: Methanol-, Ethanol- und Benzolflamme ohne Spektralbrille bei Tageslicht betrachtet; unten, von links nach rechts: Ethanol- und Benzolflamme im verdunkelten Raum durch Spektralbrille betrachtet
Die obere Reihe in Bild 24 zeigt die Diffusionsflamme von Methanol, Ethanol und Benzol bei Tageslicht. Die Methanolflamme rußt nicht, sie ist daher transparent. Die Ethanolflamme rußt wenig und ist halb-transparent. Die Benzolflamme rußt stark und ist undurchsichtig. In der unteren Reihe zeigt das linke Bild die schwach-rußende Ethanolflamme mit pastellfarbenen Regenbogen, während die stark rußende Benzolflamme (Bild unten rechts) kräftige Regenbogenfarben produziert.








Bild 25: Flammen von Kaminanzündern; obere Reihe: rapsölhaltiger Bio-Kaminanzünder;
untere Reihe: paraffinhaltiger Kaminanzünder; von links nach rechts: Flamme in verdunkeltem Raum und bei Tageslicht, Flammenbild jeweils ohne und mit Spektralbrille fotografiert.
Bild 25 zeigt Flammen von rapsölhaltigem Bio-Kaminanzünder (obere Reihe) und paraffinhaltigem Kaminanzünder. Die Bioanzünder-Flamme brennt mit einer Temperatur von ca. 1250 – 1280 °C, die Paraffinanzünder-Flamme mit ca. 1300 – 1320 °C. Die Paraffinanzünder- Verbrennung verläuft doppelt so schnell wie die der Bioanzünder. Die Bioanzünder-Flamme rußt wenig, die Flamme des Paraffin-Anzünders stark.
Die in Bild 22 gezeigte Butan-Diffusionsflamme rußt kräftig, wenn die Flamme mit einem Gegenstand abgekühlt wird, während die ungestörte Flamme keine Rußentwicklung zeigt. Die Erklärung hierfür ist folgende: Im Luftmangelbereich der Diffusionsflamme (meist in der Flammenmitte, s. Bilder 6, 7) bildet sich Ruß, der im Luftüberschussbereich oft verbrennt. Wird die Flamme abrupt abgekühlt, kann der Ruß nicht verbrennen und wird als dunkler Rauch sichtbar. Ähnliches passiert in Kaminöfen bei ungünstigem Anfachen des Feuers und bei Durchbrandfeuerung. Beim falschen Anfachen entweicht starker Rauch aus dem Schornstein, da die Flamme der angezündeten kleinen Holzstücke durch die draufgelegten großen Holzstücke abrupt abgekühlt wird, wie gezeigt in Bild 26, obere Bilderreihe. Beim Anfeuern ohne Rauch werden die großen Holzstücke unten und die kleinen oben in den Ofen gelegt, und das Feuer wird oben angezündet (Bild 26, untere Bilderreihe).







Bild 26: Falsches (obere Bilderreihe) und richtiges
Anfachen (untere Bilderreihe) des Kaminfeuers (Quelle: Feuern ohne Rauch,
Energie Schweiz, Publikation Nr. 315 ) www.holzenergie.ch/fileadmin/user_resources/publications/315_RichtigAnfeuernObAbbrand_NEU_D.pdf

Bild 27 zeigt die Anzündphase von 4 kg Stückholz mit der Züricher Anfeuermethode. Die kleinen Holzstücke brennen bereits, ihre Flamme kann ungestört im Feuerraum aufsteigen, ohne durch kalte Holzstücke passieren zu müssen. Feuerraumwand und Glasscheibe bleiben annähernd rußfrei. Die Entwicklung des Abbrandes kann in Bild 28 und 29 verfolgt werden. Die linken zwei Fotos des Bildes 28 zeigen die Flamme nach 20 Minuten Brennzeit, die rechten zwei Fotos nach 40 Minuten. Von den Bilderpaaren zeigt das jeweilige linke Foto das Feuer mit bloßem Auge und das rechte Foto durch die Spektralbrille betrachtet.




Bild 28: Zeitliche Entwicklung des Feuers; linkes Bilderpaar – Flamme nach 20 Minuten Brennzeit,
rechtes Bilderpaar – Flamme nach 40 Minuten.


Bild 29: Flamme nach 50 Minuten Brennzeit. Links: Flamme mit bloßem Auge betrachtet,
rechts: Flamme durch Spektralbrille.
In der Bilderserie 27 bis 29 ist der zeitliche Ablauf einer Feuerung kurz zusammengefasst. Das Feuer brennt im oberen-Abbrand-Modus (Bild 3) deutlich langsamer als beim Durchbrand, wodurch die Wärmeabgabe des Ofens an den Wärmebedarf des beheizten Raumes besser
angepasst wird. Das linke Bilderpaar in Bild 28 zeigt die Flamme in der Entgasungsphase. Durch die starke Rußbildung ist die Flamme undurchsichtig, die Luftzahl beträgt etwa λ≈2. Das Bild durch die Spektralbrille zeigt kräftige Regenbogenfarben. Das rechte Bilderpaar (Brenndauer ca. 40 Minuten) zeigt das Feuer in der Vergasungsphase. Die Rußbildung ist weitgehend zurückgegangen, die Flamme ist halbtransparent, in der Mitte des unteren Bild-Drittels ist die blaue Grundfarbe der Flamme erkennbar. Das Bild durch die Spektralbrille zeigt einen pastellfarbigen Regenbogen. Die Luftzahl beträgt etwa λ≈3. Bild 29 zeigt das Feuer am Ende der Vergasungsphase. Es findet keine Rußbildung mehr statt, die Rußzahl ist Rz = 0. Die gelbe Farbe im Spektralbild kommt durch Flammenfärbung des Natriums in der Asche zustande (siehe Bild 20). Die Luftzahl der Verbrennung beträgt in dieser Phase etwa λ≈4,5.